- 醫(yī)療器械注冊
- 第二類醫(yī)療器械注冊 第三類醫(yī)療器械注冊 進口醫(yī)療器械注冊 第一類醫(yī)療器械備案 體外診斷試劑注冊 醫(yī)療器械產品技術要求 醫(yī)療器械生產許可證
- 醫(yī)療器械CE認證
- 醫(yī)療器械CE認證 FDA注冊(備案) 醫(yī)療器械境外注冊服務 ISO13485認證 ISO15378醫(yī)療包材體系認證 MDSAP認證服務 ISO13485內審員培訓
- 醫(yī)療器械臨床試驗
- 醫(yī)療器械臨床試驗服務 同品種比對臨床評價 體外診斷試劑(IVD)臨床試驗服務 臨床協調員(CRC)服務 進口醫(yī)療器械補充臨床試驗服務 醫(yī)院臨床試驗機構備案服務 醫(yī)療器械可用性工程文檔編制
- 醫(yī)療器械經營許可
- 醫(yī)療器械經營許可證辦理 第二類醫(yī)療器械經營備案 醫(yī)療器械網絡銷售備案 醫(yī)療器械分類界定代辦 醫(yī)療器械飛行檢查服務 醫(yī)療器械主文檔登記代辦 醫(yī)療器械創(chuàng)新申報代辦
- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
一文讀懂體外診斷試劑變更注冊申報資料要求(2025年最新IVD變更注冊) 對于體外診斷試劑變更注冊事項來說,難度介于體外診斷試劑首次注冊和體外診斷試劑延續(xù)注冊中間,更接近于體外診斷時間注冊注冊,本文為大家介紹2025年度最新IVD變更注冊申報資料要求,一起看正文。 時間:2025-10-5 21:20:20 瀏覽量:235

-
一文讀懂體外診斷試劑注冊申報資料要求解讀(2025年最新IVD產品申報要求)-下 對于體外診斷試劑注冊項目來說,體外診斷試劑注冊申報資料是IVD研發(fā)、制造和質量保證的精要表達,體外診斷試劑注冊資料的要求細致、專業(yè)、系統(tǒng)化。寫個文章為大家說說體外診斷試劑注冊申報資料要求解讀(2025年最新IVD產品申報要求)下半部分,一起看正文。 時間:2025-9-24 22:33:03 瀏覽量:192

-
一文讀懂體外診斷試劑注冊申報資料要求解讀(2025年最新IVD產品申報要求)-上 對于體外診斷試劑注冊項目來說,體外診斷試劑注冊申報資料是IVD研發(fā)、制造和質量保證的精要表達,體外診斷試劑注冊資料的要求細致、專業(yè)、系統(tǒng)化。寫個文章為大家說說體外診斷試劑注冊申報資料要求解讀(2025年最新IVD產品申報要求)上半部分,一起看正文。 時間:2025-9-24 22:24:52 瀏覽量:254

-
浙江省第二類體外診斷試劑注冊常見問題答疑 在第二類醫(yī)療器械技術審評和注冊咨詢中,我們發(fā)現部分企業(yè)對醫(yī)療器械注冊法規(guī)和標準要求、申報資料準備、研究評價標準和方法仍缺乏認識和了解,現將技術審評發(fā)補中的常見問題以及日常咨詢中的共性問題進行梳理,希望能讓大家更直觀、更詳細地了解相關技術審評要求,不斷提升浙江省第二類醫(yī)療器械注冊申報的質量和效率。 時間:2025-2-21 22:24:17 瀏覽量:1361

-
第二類體外診斷試劑產品注冊通用指導原則有哪些? 截至2024年3月29日,醫(yī)療器械注冊人申報第二類體外診斷試劑產品注冊時,常用的通用指導原則有哪些?詳見正文,建議大家收藏哦! 時間:2024-3-29 21:18:40 瀏覽量:3652

-
第二類體外診斷試劑產品注冊常用通用標準有哪些? 截至2024年3月29日,申報第二類體外診斷試劑產品注冊時常用通用標準有哪些?一起看正文。建議小伙伴們收藏哦! 時間:2024-3-29 21:11:15 瀏覽量:3546

-
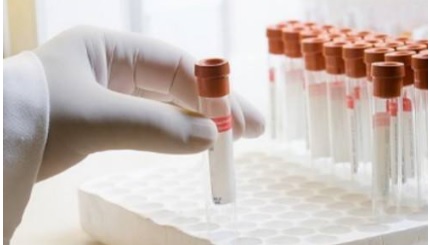
體外診斷試劑穩(wěn)定性研究注冊審查指導原則(征求意見稿) 2023年12月01日,國家藥監(jiān)局發(fā)布《體外診斷試劑穩(wěn)定性研究注冊審查指導原則(征求意見稿)》,本指導原則旨在指導體外診斷試劑注冊申請人對體外診斷試劑穩(wěn)定性進行充分的研究,并整理形成體外診斷試劑注冊申報資料,同時也為技術審評部門審評注冊申報資料提供參考。 時間:2023-12-3 10:40:12 瀏覽量:4195
-
體外診斷試劑產品技術要求模板(三類定性試劑) 體外診斷試劑產品技術要求因其管理類別、作用機理、定性或定量檢測、預期用途等不同,略有差異,本位以第三類定性體外診斷試劑為例,提供了一個體外診斷試劑產品技術要求模板,供學習、參考使用。 時間:2022-9-4 15:19:12 瀏覽量:4555

-
新型冠狀病毒(2019-nCoV)抗原檢測試劑注冊審查指導原則(2022年第18號) 2022年4月27日,為進一步規(guī)范新型冠狀病毒相關檢測試劑的管理,國家藥監(jiān)局器審中心組織制定并發(fā)布了《新型冠狀病毒(2019-nCoV)抗原檢測試劑注冊審查指導原則》(2022年第18號),詳見正文。 時間:2022-4-28 14:38:08 瀏覽量:6329
-
新型冠狀病毒(2019-nCoV)抗體檢測試劑注冊審查指導原則(2022年第18號) 2022年4月27日,為進一步規(guī)范新型冠狀病毒相關檢測試劑的管理,國家藥監(jiān)局器審中心組織制定并發(fā)布了《新型冠狀病毒(2019-nCoV)抗體檢測試劑注冊審查指導原則》(2022年第18號),詳見正文。 時間:2022-4-28 14:32:53 瀏覽量:3889

-
新型冠狀病毒(2019-nCoV)核酸檢測試劑注冊審查指導原則(2022年第18號) 2022年4月27日,為進一步規(guī)范新型冠狀病毒相關檢測試劑的管理,國家藥監(jiān)局器審中心組織制定并發(fā)布了《新型冠狀病毒(2019-nCoV)核酸檢測試劑注冊審查指導原則》,詳見正文。 時間:2022-4-28 14:27:18 瀏覽量:5182
-
醫(yī)療器械注冊證(體外診斷試劑)內容和格式 醫(yī)療器械注冊證(體外診斷試劑)內容和格式 時間:2021-10-4 11:45:31 瀏覽量:4360

-
體外診斷試劑生產質量體系檢查要點指南(2017年修訂版) 體外診斷試劑生產質量體系檢查要點指南(2017年修訂版) 時間:2021-8-8 15:32:26 瀏覽量:4849

-
體外診斷試劑注冊基本要求 體外診斷試劑注冊與醫(yī)療器械注冊整體流程大致一樣,但考慮到體外診斷試劑無論是風險還是使用方面與醫(yī)療器械又存在部分差異,體外診斷試劑注冊資料更多要求研發(fā)人員編制,因此,體外診斷試劑與醫(yī)療器械注冊存在差異。我們一起來了解一下體外診斷試劑注冊基本要求。 時間:2019-10-4 11:03:50 瀏覽量:8307