- 新聞動態(tài)
- 醫(yī)療器械注冊
- 醫(yī)療器械CE認證
- 醫(yī)療器械臨床試驗
- 醫(yī)療器械經(jīng)營許可
- 聯(lián)系我們

聯(lián)系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
三維電子腹腔鏡注冊及醫(yī)療器械臨床評價要點 三維電子腹腔鏡與內(nèi)窺鏡圖像處理主機連接,在醫(yī)療機構(gòu)中使用,通過創(chuàng)口進入人 體,用于腹腔手術(shù)中的觀察成像,三維電子腹腔鏡由插入部、手持部、內(nèi)窺鏡視頻線纜組成,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。本文為大家介紹三維電子腹腔鏡注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-8-9 0:00:00 瀏覽量:334

-
2025年6月國家局批準105項進口第一類醫(yī)療器械產(chǎn)品備案 來自國家藥監(jiān)局2025年8月8日公開披露的消息,2025年6月國家藥監(jiān)局批準進口第一類醫(yī)療器械產(chǎn)品備案事項105項,其中包括lpha-1-Fetoprotein抗體試劑(免疫組織化學(xué))、Hepatocyte抗體試劑(免疫組織化學(xué))、噴劑敷料、液體傷口敷料、乳頭皸裂傷口護理軟膏包、妊娠紋傷口護理軟膏包等眾多進口第一類醫(yī)療器械產(chǎn)品,一起來看具體內(nèi)容。 時間:2025-8-9 0:00:00 瀏覽量:354

-
免驗配或自驗配的助聽器是否可以免于進行臨床評價? 對于醫(yī)療器械注冊人來說,在醫(yī)療器械注冊項目前期都會考慮產(chǎn)品是否可以免于醫(yī)療器械臨床評價,是否可以免于醫(yī)療器械臨床試驗,對于這個事項,一定要關(guān)注法規(guī)及免臨床目錄。本文以助聽器產(chǎn)品為例為大家說說這個事。 時間:2025-8-7 0:00:00 瀏覽量:335

-
醫(yī)療器械設(shè)備驅(qū)動軟件直接購買現(xiàn)成軟件,是否要提供該軟件的研究報告? 多數(shù)有源醫(yī)療器械注冊產(chǎn)品離不開軟件,多數(shù)有源醫(yī)療器械設(shè)備都含有軟件,比如驅(qū)動軟件,比如控制軟件。本文為大家說說醫(yī)療器械設(shè)備驅(qū)動軟件直接購買供應(yīng)商生產(chǎn)的現(xiàn)成軟件,醫(yī)療器械注冊人是否需要提供該驅(qū)動軟件的研究報告?一起看正文。 時間:2025-8-7 0:00:00 瀏覽量:345

-
醫(yī)療器械發(fā)生變化時,何種情況需對其生物安全性進行重新評價? 對于醫(yī)療器械注冊產(chǎn)品來說,取得醫(yī)療器械注冊證之后發(fā)生變化是常見情況,但是企業(yè)需要特別注意對變化的處理,稍有不慎就會涉及違規(guī)。本文為大家說說醫(yī)療器械發(fā)生變化時,需對其生物安全性進行重新評價的情形,一起看正文。 時間:2025-8-6 21:57:17 瀏覽量:315

-
牙科鉆頭產(chǎn)品注冊單元應(yīng)如何劃分? 配合牙科種植手機使用,用于口腔中牙槽骨等硬質(zhì)結(jié)構(gòu)的切、削、鉆等操作的牙科鉆頭,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。牙科鉆頭根據(jù)使用功能分為非導(dǎo)板牙科鉆頭(先鋒鉆、擴孔鉆、成形鉆、取骨鉆、片切鉆、修整鉆)和導(dǎo)板牙科鉆頭(導(dǎo)板先鋒鉆、導(dǎo)板擴孔鉆、導(dǎo)板成形鉆)。本文為大家介紹牙科鉆頭產(chǎn)品注冊單元劃分,一起看正文。 時間:2025-8-6 0:00:00 瀏覽量:367

-
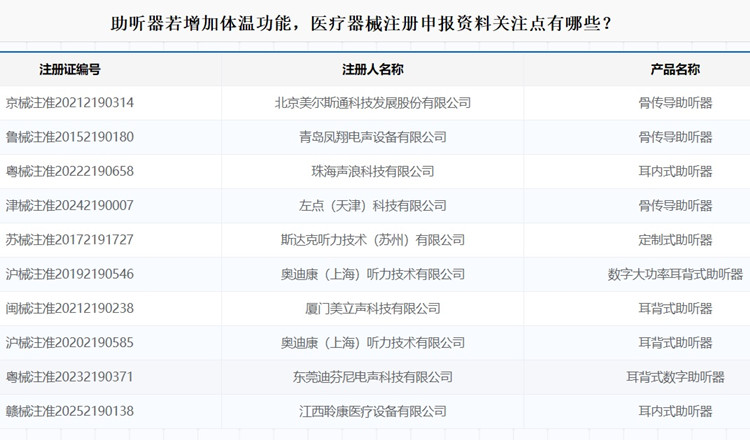
助聽器若增加體溫功能,醫(yī)療器械注冊申報資料關(guān)注點有哪些? 供聽力障礙者補償聽力用的助聽器在我國屬于第二類醫(yī)療器械注冊,是臨床最常見醫(yī)療器械產(chǎn)品之一。隨著技術(shù)的進步,及患者需求逐漸超越臨床需求,醫(yī)療器械的功能和設(shè)計越來越帶有審美、帶有溫度、帶有個性。今天來給大家說個具體問題,即助聽器若增加體溫功能,注冊申報資料中的關(guān)注點有哪些?一起看正文。 時間:2025-8-5 0:00:00 瀏覽量:329
-
2025年7月浙江省第二類醫(yī)療器械注冊審評情況 來自浙江省藥品監(jiān)督管理局近日公開披露的消息,一起來看2025年7月浙江省第二類醫(yī)療器械注冊審評情況,了解官網(wǎng)口徑的真實數(shù)據(jù)。 時間:2025-8-5 0:00:00 瀏覽量:341

-
一次性使用內(nèi)窺鏡噴灑管注冊及醫(yī)療器械臨床評價要點 手術(shù)中在內(nèi)窺鏡下操作,進行液體輸送、灌洗、藥液噴灑。不用于血液循環(huán)系統(tǒng)和中樞神經(jīng)系統(tǒng)給物的一次性使用內(nèi)窺鏡噴灑管,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品,一次性使用內(nèi)窺鏡噴灑管根據(jù)結(jié)構(gòu)不同分為極簡型(J)和標準型(B)兩種,按噴 頭型式分為霧狀噴頭(W)和直線噴頭(Z)兩種。本文為大家介紹一次性使用內(nèi)窺鏡噴灑管注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-8-4 0:00:00 瀏覽量:423

-
一次性使用管型吻合器注冊及醫(yī)療器械臨床評價要點 用于食管、胃、腸等消化道重建手術(shù)中消化道的端端、端側(cè)和側(cè)側(cè)吻合的一次性使用管型吻合器,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。一次性使用管型吻合器由抵釘座、釘倉、套管、保險、活動手柄 、調(diào)節(jié)螺母、吻合 釘、環(huán)形刀、墊刀圈、保護蓋組成,附件為荷包接桿。產(chǎn)品以無菌狀態(tài)提供,經(jīng)環(huán) 氧乙烷滅菌,一次性使用。本文為大家介紹一次性使用管型吻合器注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-8-4 0:00:00 瀏覽量:385

-
醫(yī)用內(nèi)窺鏡熒光冷光源注冊及醫(yī)療器械臨床評價要點 在醫(yī)療機構(gòu)中使用,用于內(nèi)窺鏡診斷和/或治療手術(shù)中,為內(nèi)窺鏡觀察人體體腔的視場區(qū)域提供觀察用照明。用于近紅外熒光成像時,需配合已在中國境內(nèi)批準上市且應(yīng)用部位一致的吲哚箐綠使用的醫(yī)用內(nèi)窺鏡熒光冷光源,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。醫(yī)用內(nèi)窺鏡熒光冷光源由主機、電源線組成。本文為大家介紹醫(yī)用內(nèi)窺鏡熒光冷光源注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-8-3 0:00:00 瀏覽量:359

-
牙科種植用鉆注冊及醫(yī)療器械臨床評價要點 用于口腔種植手術(shù)過程中,制備與所用種植體相匹配的種植窩洞預(yù)備孔的牙科種植用鉆,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。牙科種植用鉆采用不銹鋼(420Mod)材料制成,產(chǎn)品為非無菌提供,表面經(jīng)過類金剛石(DLC)涂層處理或未經(jīng)表面處理,重復(fù)使用,使用前由醫(yī)療機構(gòu)按要求進行清潔滅菌處理。本文為大家介紹牙科種植用鉆注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-8-3 0:00:00 瀏覽量:356

-
重組膠原蛋白無菌敷貼注冊及醫(yī)療器械同品種比對臨床評價要點 適用于非慢性創(chuàng)面(如淺表性創(chuàng)面、小創(chuàng)口、激光/光子/果酸換膚/微整形術(shù)后創(chuàng)面)及周圍皮膚的護理,為創(chuàng)面愈合提供微環(huán)境的重組膠原蛋白無菌敷貼,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。重組膠原蛋白無菌敷貼由重組膠原蛋白、甘油、卡波姆、三乙醇胺、苯氧乙醇、純化水和無紡布組成,經(jīng)鋁箔袋封裝而成。該產(chǎn)品以無菌狀態(tài)提供,經(jīng)輻射滅菌,一次性使用。本文為大家介紹重組膠原蛋白無菌敷貼注冊及醫(yī)療器械臨床評價要點。 時間:2025-7-31 0:00:00 瀏覽量:460

-
一氧化氮檢測器注冊及醫(yī)療器械臨床評價要點 配合呼氣分析儀使用,用于檢測呼出氣 NO(一氧化氮)濃度的一氧化氮檢測器,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。一氧化氮檢測器由外殼、硬件接口卡、一氧化氮傳感器組成。本文為大家介紹一氧化氮檢測器注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-7-31 0:00:00 瀏覽量:355

-
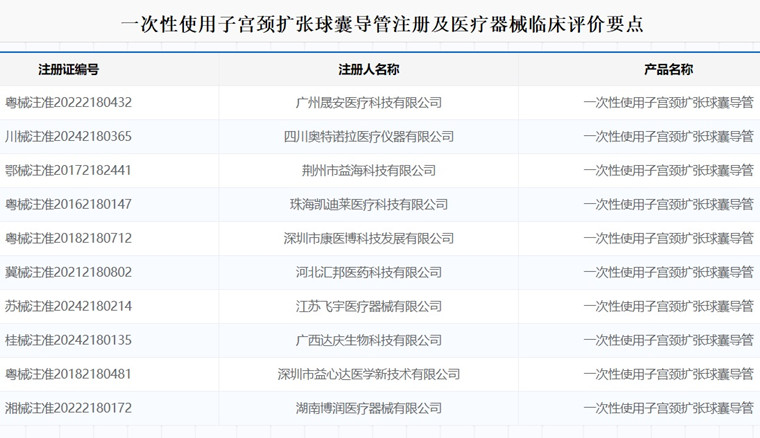
一次性使用子宮頸擴張球囊導(dǎo)管注冊及醫(yī)療器械臨床評價要點 用于機械擴張子宮頸的一次性使用子宮頸擴張球囊導(dǎo)管,在我國屬于二類無菌醫(yī)療器械注冊產(chǎn)品。一次性使用子宮頸擴張球囊導(dǎo)管單球囊由導(dǎo)管頭端、子宮球囊、導(dǎo)管、單向閥、鎖 緊環(huán)組成;雙球囊由導(dǎo)管頭端、子宮球囊、陰道球囊、導(dǎo)管、單向閥、鎖緊環(huán)、針 芯(選配)組成。產(chǎn)品以無菌狀態(tài)提供,經(jīng)環(huán)氧乙烷滅菌,一次性使用。本文為大家介紹一次性使用子宮頸擴張球囊導(dǎo)管注冊及醫(yī)療器械臨床評價要點。 時間:2025-7-29 0:00:00 瀏覽量:710
-
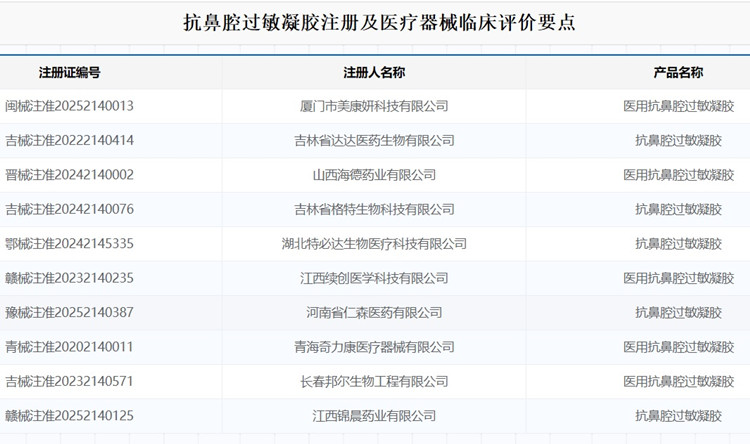
抗鼻腔過敏凝膠注冊及醫(yī)療器械臨床評價要點 用于過敏性鼻炎患者、過敏性哮喘患者,通過阻隔致病性微生物及其他顆粒性過敏 物質(zhì)進入鼻腔,緩解因過敏性鼻炎、過敏性哮喘引發(fā)的相關(guān)癥狀。抗鼻腔過敏凝膠在我國屬于第二類醫(yī)療器械注冊產(chǎn)品。抗鼻腔過敏凝膠由羥丙甲纖維素、黃原膠、甘油、檸檬酸、羥苯甲酯、羥苯丙酯、 純化水制成,凝膠封裝于鋁塑包裝內(nèi);產(chǎn)品以非無菌狀態(tài)提供。本文為大家介紹抗鼻腔過敏凝膠注冊及醫(yī)療器械臨床評價要點。 時間:2025-7-29 0:00:00 瀏覽量:1208
-
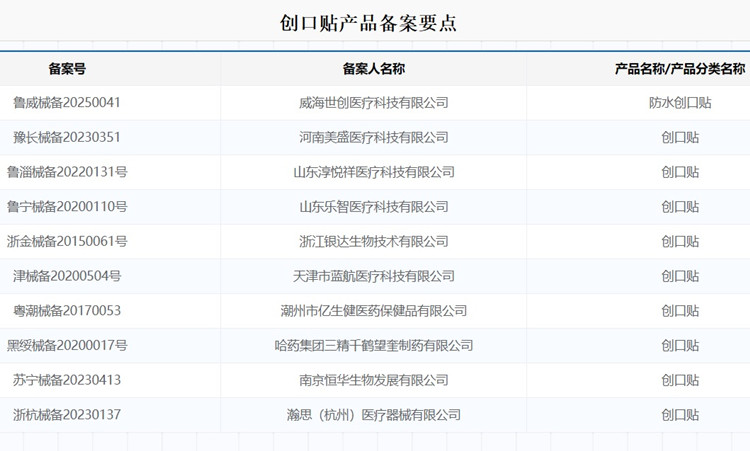
創(chuàng)口貼產(chǎn)品備案要點 創(chuàng)口貼(14-10-02)是最廣為認知的第一類醫(yī)療器械備案產(chǎn)品之一,用于真皮淺層及其以上的淺表性小創(chuàng)傷、擦傷等,為淺表創(chuàng)面、皮膚損傷提供愈合環(huán)境。創(chuàng)口貼也是應(yīng)用最廣的第一類醫(yī)療器械之一,本文為大家介紹創(chuàng)口貼產(chǎn)品備案要點,一起看正文。 時間:2025-7-28 0:00:00 瀏覽量:483
-
第一類醫(yī)療器械備案注意事項(導(dǎo)光凝膠備案) 導(dǎo)光凝膠(09-03-08)在我國按照第一類醫(yī)療器械備案管理,由瓶體(管體)、凝膠組成。凝膠采用卡波姆、聚丙烯酸脂、甘油、三乙醇胺、石墨烯、水、山梨酸鉀組成。產(chǎn)品不含有發(fā)揮藥理學(xué)、免疫學(xué)或者代謝作用的成分,不包含附錄所列成分。非無菌產(chǎn)品。用于光子治療過程中隔熱和導(dǎo)光,與光子治療設(shè)備配合使用。本文為大家說說導(dǎo)光凝膠備案注意事項。 時間:2025-7-28 0:00:00 瀏覽量:498

-
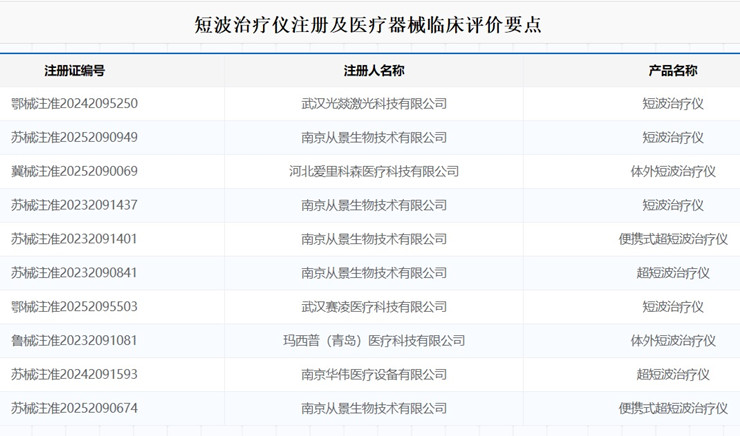
短波治療儀注冊及醫(yī)療器械臨床評價要點 利用短波能量對身體組織(含盆底肌肉)加熱,起到溫熱效果的短波治療儀,在我國屬于第二類醫(yī)療器械注冊產(chǎn)品,短波治療儀產(chǎn)品由主機、電極、電源線、一次性電極傳導(dǎo)器(配合電極使用)和選配件(通訊 模塊和體表電極)組成。本文為大家介紹短波治療儀注冊及醫(yī)療器械臨床評價要點,一起看正文。 時間:2025-7-27 20:06:09 瀏覽量:476
-
銷售家用制氧機需要辦理第二類醫(yī)療器械經(jīng)營備案憑證嗎? 對于家用制氧機是否需要辦理第二類醫(yī)療器械經(jīng)營備案憑證?這是個問題,直接回答是否者不是都是個問題,需要具體情況具體分析,經(jīng)營家用制氧機的企業(yè)務(wù)必要留意。 時間:2025-7-27 19:58:21 瀏覽量:427

