- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
醫療器械臨床試驗樣品如何管理 當今,隨著新的GCP法規的全面實施,并伴隨著各項監督抽查在全國范圍內陸續開展,醫療器械臨床試驗的各種規定越來越嚴格了。除了過程中試驗的質量必須得到有效的控制外,整個試驗樣品的管理也是一個至關重要的方面。 時間:2019-7-30 23:34:38 瀏覽量:5791

-
醫療器械臨床試驗注意事項簡介 醫療器械臨床試驗是對申辦方申請注冊的醫療器械臨床試用或驗證的過程。了解醫療器械臨床試驗注意事項,在進行注冊的時候,對企業來說是很重要的。 時間:2019-7-29 23:46:42 瀏覽量:3990

-
醫療器械臨床試驗相關問題官方解答 依據《醫療器械監督管理條例》,醫療器械注冊前需進行臨床評價并提交臨床評價資料,通過開展臨床試驗進行臨床評價的,其臨床試驗應按照醫療器械臨床試驗法規及相關規范要求,在有資質的臨床試驗機構進行,并向臨床試驗主管部門提出備案或審批申請。 時間:2019-7-28 22:41:45 瀏覽量:4092

-
醫療器械臨床試驗管理規范GCP應當遵循的基本原則是什么? ICH-GCP是藥品國際注冊中共認的GCP。ICH-GCP列出的13條基本原則是GCP的科學性和倫理性原則的集中體現,是ICH-GCP的精華所在。隨著我國藥品審評審批制度改革的深入推進,我國GCP與ICH-GCP全面接軌已經是大勢所趨。與藥物開發要求一致,醫療器械臨床試驗的實施也應當遵循倫理原則、科學原則以及依法原則,即遵循GCP及相關 法規的要求。 時間:2019-7-27 1:05:34 瀏覽量:14021

-
醫療器械臨床試驗CRF設計流程和CDASH介紹 ICH-GCP將病例報告表(CRF)定義為一種印刷的、可視的或者是電子版的文件,用于記錄每個受試者的所有試驗方案要求的信息,向申辦者報告,CRF是醫療器械臨床試驗數據采集重要的必備工具。 時間:2019-7-25 23:19:52 瀏覽量:8956

-
醫療器械臨床試驗問答之1-5 醫療器械臨床試驗是指:獲得醫療器械臨床試驗資格的醫療機構(以下稱醫療機構)對申請注冊的醫療器械在正常使用條件下的安全性和有效性按照規定進行試用或驗證的過程。醫療器械臨床試驗的目的是評價受試產品是否具有預期的安全性和有效性 。 時間:2019-7-24 22:37:22 瀏覽量:2952

-
山東省醫療器械臨床試驗管理備案 醫療器械臨床試驗備案申請實行“全程網辦”,申請人需通過山東省食品藥品監督管理局企業行政許可服務平臺提交有關材料進行備案。 時間:2019-7-24 0:19:14 瀏覽量:8040

-
廣東省藥品監督管理局關于開展2019年第一期醫療器械臨床試驗監督抽查的通告 為貫徹實施中共中央辦公廳、國務院辦公廳《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),加強醫療器械臨床試驗監督管理,根據2019年重點工作安排,廣東省藥品監督管理局抽取D-二聚體(D-Dimer)測定試劑盒(化學發光免疫分析法)(備案號:粵械臨備20180264)等5個醫療器械臨床試驗項目(見附件),將對其臨床試驗過程的真實性和規范性開展現場監督檢查。 時間:2019-7-21 22:55:05 瀏覽量:2922

-
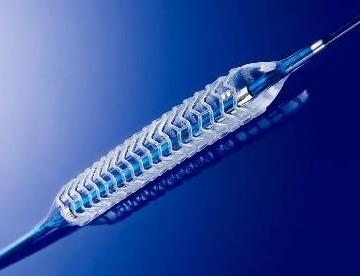
醫療器械臨床試驗 之 《冠狀動脈藥物洗脫支架臨床試驗指導原則(2018年第21號)》 去年,藥監局發布了《冠狀動脈藥物洗脫支架臨床試驗指導原則》。本指導原則適用于《醫療器械注冊管理辦法》規定需在中國境內進行臨床試驗的冠狀動脈藥物洗脫支架。本指導原則適用于所含藥物屬化學藥物,以金屬支架為支架平臺的冠狀動脈藥物洗脫支架的臨床試驗。 時間:2019-7-20 23:10:13 瀏覽量:3966
-
3個醫療器械臨床試驗涉嫌造假被查處 近日,國家食藥監總局公布第二批醫療器械臨床試驗監督抽查結果,檢查發現3個醫療器械注冊申請項目的臨床試驗存在真實性問題。 時間:2019-7-19 23:36:45 瀏覽量:3285

-
醫療器械臨床試驗11個常見問題解答 醫療器械臨床試驗是指:獲得醫療器械臨床試驗資格的醫療機構(以下稱醫療機構)對申請注冊的醫療器械在正常使用條件下的安全性和有效性按照規定進行試用或驗證的過程。醫療器械臨床試驗的目的是評價受試產品是否具有預期的安全性和有效性 。 時間:2019-7-18 22:40:33 瀏覽量:3850

-
醫療器械臨床試驗審批申報資料要求及說明 為規范醫療器械注冊管理,指導企業做好注冊申報工作,根據《醫療器械監督管理條例》(國務院令第650號)和《醫療器械注冊管理辦法》(國家食品藥品監督管理總局令第4號),總局組織制定了醫療器械注冊申報資料要求和批準證明文件格式(見附件1—8),現予公布,自2014年10月1日起施行。 時間:2019-7-18 0:41:55 瀏覽量:5547

-
《醫療器械臨床試驗審批項目立卷審查要求(試行)》 為貫徹落實中共中央辦公廳、國務院辦公廳《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),配合醫療器械注冊電子申報工作的開展,國家藥監局2019年07月10日發布《醫療器械臨床試驗審批項目立卷審查要求(試行)》,自2019年9月1日起實施。 時間:2019-7-16 22:39:29 瀏覽量:3680

-
醫療器械臨床試驗 之 《人工晶狀體臨床試驗指導原則(2019年第13號)》 為了進一步規范人工晶狀體產品上市前的臨床試驗,并指導該類產品申請人在申請產品注冊時臨床試驗資料的準備,根據《醫療器械臨床試驗質量管理規范》,撰寫本臨床試驗指導原則。 時間:2019-7-16 1:05:23 瀏覽量:3155

-
無源植入性醫療器械臨床試驗審批 申報資料編寫指導原則 為貫徹實施中共中央辦公廳 國務院辦公廳《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》(廳字〔2017〕42號),加強醫療器械臨床試驗監督管理,進一步提高注冊審查質量,根據《關于公布醫療器械注冊申報資料要求和批準證明文件格式的公告》(國家食品藥品監督管理總局公告2014年第43號)要求,國家藥品監督管理局組織制定、發布了《無源植入性醫療器械臨床試驗審批申報資料編寫指導原則》。 時間:2019-7-14 23:58:02 瀏覽量:3415

-
滬藥監局開展醫療器械臨床試驗調研 近日,上海市藥監局副局長郭術廷帶隊赴上海交通大學醫學院附屬仁濟醫院,對醫院臨床研究、醫療器械臨床試驗以及拓展性臨床試驗等方面開展調研并座談。仁濟醫院科研處、機構辦和醫療一線的臨床部門部分專家參與座談。 時間:2019-7-13 0:00:00 瀏覽量:3107

-
醫療器械臨床試驗知情同意:每個受試者最基本的權利 知情同意權包括兩個部分,第一是對試驗相關信息詳細獲取的權利,即:知情權,它使受試者的生命健康得以保證;第二是對是否參與做出自主選擇的權利,即自主選擇權,它使受試者的人格尊嚴得到實現。 時間:2019-7-12 22:43:58 瀏覽量:5728

-
【醫療器械臨床試驗基礎知識分享】不良事件、嚴重不良事件和不良反應 不良事件(AE)是指在醫療器械臨床試驗或藥物臨床試驗中受試者發生的任何可能與試驗治療及試驗用藥品/醫療器械有關或不一定有關的醫療事件。 時間:2019-7-11 23:20:46 瀏覽量:22293

-
醫療器械臨床試驗現場檢查要點(體外診斷試劑) 根據《醫療器械監督管理條例》、《體外診斷試劑注冊管理辦法》和體外診斷試劑臨床試驗(研究)技術指導原則等相關要求,國家食品藥品監督管理總局制訂了《醫療器械臨床試驗現場檢查要點(2016年)》(體外診斷試劑)。2016年6月8號,國家食品藥品監督管理總局發布了總局關于開展醫療器械臨床試驗監督抽查工作的通告。 時間:2019-7-10 0:00:00 瀏覽量:6538

-
醫療器械臨床試驗研究者文件夾(ISF)該如何管理? 研究者文件夾應該包括試驗方案、研究者手冊、CRF、ICF、篩入選表、受試者鑒認代碼表、器械發放回收記錄、器械的說明書以及檢驗報告。 時間:2019-7-9 23:30:12 瀏覽量:28841

