- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
有源醫療器械注冊申報資料(首次注冊)要求解讀(下) 對于有源醫療器械注冊產品來說,注冊資料相對無源產品可能會更加復雜、多變,涉及的知識范疇也可能更廣,本文為大家帶來有源醫療器械注冊申報資料(首次注冊)要求解讀,考慮到文章篇幅,今天繼續為大家帶來后下部分內容,包括風險管理、醫療器械安全和性能基本原則(EP)清單、產品技術要求、醫療器械注冊檢驗報告、非臨床研究等內容,一起看正文。 時間:2025-9-8 0:00:00 瀏覽量:302

-
有源醫療器械注冊申報資料(首次注冊)要求解讀(中) 對于有源醫療器械注冊產品來說,注冊資料相對無源產品可能會更加復雜、多變,涉及的知識范疇也可能更廣,本文為大家帶來有源醫療器械注冊申報資料(首次注冊)要求解讀,考慮到文章篇幅,分上中下三部門為大家呈現,本文為大家帶來中部分內容,一起看正文。 時間:2025-9-7 0:00:00 瀏覽量:294

-
有源醫療器械注冊申報資料(首次注冊)要求解讀(上) 對于有源醫療器械注冊產品來說,注冊資料相對無源產品可能會更加復雜、多變,涉及的知識范疇也可能更廣,本文為大家帶來有源醫療器械注冊申報資料(首次注冊)要求解讀,考慮到文章篇幅,分上中下三部門為大家呈現,先來看上部門內容。 時間:2025-9-7 20:39:23 瀏覽量:308

-
北京市創新醫療器械特別審查程序 第一條 為了保障醫療器械的安全、有效,鼓勵醫療器械創新研發,促進醫療器械新技術的推廣和應用,提高北京市醫療器械審評審批質效,促進醫療器械產業高質量發展,根據《醫療器械監督管理條例》《醫療器械注冊與備案管理辦法》《體外診斷試劑注冊與備案管理辦法》《創新醫療器械特別審查程序》和《北京市醫療器械快速審評審批辦法》等,制定本程序。 時間:2025-9-6 0:00:00 瀏覽量:315

-
北京市醫療器械快速審評審批辦法(京藥監發〔2025〕114號) 為進一步提升我市醫療器械審評審批效率,加大釋放創新開放市場活力,助力發展新質生產力,服務首都醫療器械產業高質量發展,我局結合工作實際及相關政策法規變化,組織修訂了《北京市醫療器械快速審評審批辦法》。關于醫療器械注冊法規,北京、上海、廣州三地經常是政策先行地,一起來看具體內容。 時間:2025-9-6 0:00:00 瀏覽量:327
-
醫療器械注冊申請人如何對源代碼進行管理? 對于醫療器械軟件注冊產品或是含有軟件的有源醫療器械注冊產品來說,醫療器械注冊申請人如何對源代碼進行管理,具體有什么要求,一起看正文。 時間:2025-9-5 20:48:03 瀏覽量:294

-
醫療器械注冊申請人進行軟件配置管理應關注什么? 醫療器械注冊崗位對人的要求特別高,不僅要有很好的口頭表達、書面表達,要有很好的組織、溝通能力,還有懂醫療器械質量管理體系,懂有源、懂無菌、懂軟件,真的是要求知識體系既博又專,所以對我來說,也是一直不敢說自己專業,也是在日拱一卒、持續精進。今天寫個文章,給大家分享醫療器械注冊申請人進行軟件配置管理要求,一起看正文。 時間:2025-9-5 20:39:12 瀏覽量:269

-
腹腔內窺鏡手術系統注冊審查指導原則 第4部分:風險管理(2025年第19號) 2025年9月4日,為進一步規范腹腔內窺鏡手術系統的管理,國家藥監局器審中心組織制定了《腹腔內窺鏡手術系統注冊審查指導原則 第4部分:風險管理》,現予發布。一起來看具體內容。 時間:2025-9-4 0:00:00 瀏覽量:432
-
預充式導管沖洗器注冊審查指導原則(2025年第18號) 2025年9月4日,為進一步規范預充式導管沖洗器的管理,國家藥監局器審中心組織制定了《預充式導管沖洗器注冊審查指導原則》,現予發布,一起來看具體內容。 時間:2025-9-4 0:00:00 瀏覽量:406

-
哪些體外診斷試劑注冊產品需要提交包容性研究資料? 對于體外診斷試劑注冊產品來說,注冊申報資料中相當比例的內容是研究資料,醫療器械注冊人需要根據產品的特性提供適宜的研究資料,本文為大家說說哪些哪些體外診斷試劑注冊產品需要提交包容性研究資料,一起看正文。 時間:2025-9-2 0:00:00 瀏覽量:339

-
體外診斷試劑說明書中【預期用途】描述有何要求? 對于體外診斷試劑注冊產品來說,預期用途的描述是說明書中非常重要的內容,本文未大家說說體外診斷試劑說明書中【預期用途】描述要求,一起看正文。 時間:2025-9-2 0:00:00 瀏覽量:357

-
2025年7月寧波市批準46項第一類醫療器械產品備案 來自浙江省藥品監督管理局近日披露的數據,2025年7月,寧波市市場監督管理局批準第一類醫療器械產品備案46項,包括手術頭架、造口皮膚保護劑、口腔手術臨時固定絲、p53抗體試劑、瑞氏染色液、醫用退熱貼、快裝手柄、醫用軋皮機、輥軸取皮刀等眾多第一類醫療器械產品,一起來看具體內容。 時間:2025-8-31 0:00:00 瀏覽量:354

-
2025年7月杭州市批準58個第一類醫療器械備案產品 來自浙江省藥品監督管理局近日披露的消息,2025年7月,浙江省各市共計批準第一類醫療器械備案產品163個,其中杭州市第一類醫療器械備案產品58個,一起來看具體內容。 時間:2025-8-31 21:53:57 瀏覽量:392

-
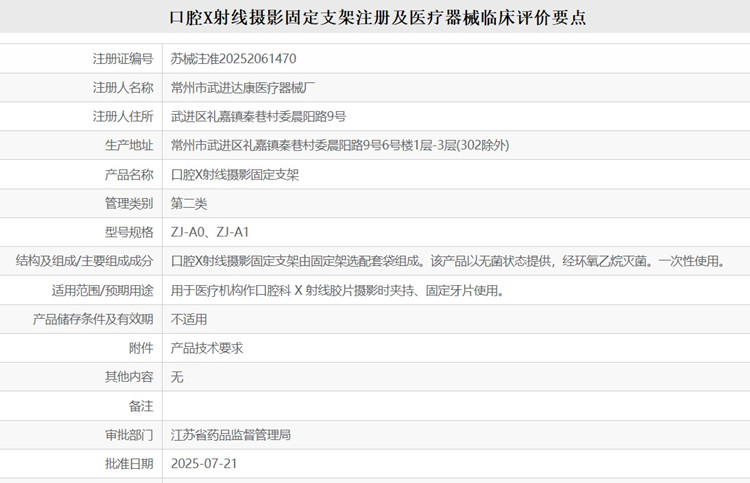
口腔 X 射線攝影固定支架注冊及醫療器械臨床評價要點 用于醫療機構作口腔科 X 射線膠片攝影時夾持、固定牙片使用的口腔 X 射線攝影固定支架,我國歸屬于第二類醫療器械注冊管理。口腔 X 射線攝影固定支架由固定架選配套袋組成。該產品以無菌狀態提供,經環氧乙烷滅菌。一次性使用。本文為大家介紹口腔 X 射線攝影固定支架注冊及醫療器械臨床評價要點,一起看正文。 時間:2025-8-30 0:00:00 瀏覽量:317
-
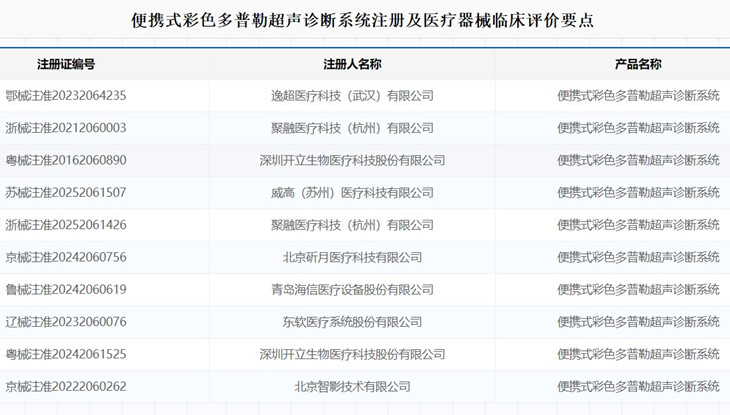
便攜式彩色多普勒超聲診斷系統注冊及醫療器械臨床評價要點 在醫療機構中,用于臨床超聲診斷檢查的便攜式彩色多普勒超聲診斷系統,在我國屬于第二類醫療器械注冊產品,產品由主機、探頭、適配器、電源線和鋰電池組成。 硬件選配包含:CW 板、移動式推車、推車電池、探頭擴展器、耦合劑加熱器、腳踏 開關、視頻轉接盒、可移動 DVD 刻錄光驅、無線網卡、穿刺架。本為便攜式彩色多普勒超聲診斷系統注冊及醫療器械臨床評價要點,一起看正文。 時間:2025-8-30 0:00:00 瀏覽量:339
-
上海市第二類創新醫療器械特別審查資料申報環節合規指引(下) 接著上一篇文章,本繼續為大家講解上海市第二類創新醫療器械特別審查資料申報環節合規指引的下半部分內容,一起看正文。 時間:2025-8-29 0:00:00 瀏覽量:313

-
上海市第二類創新醫療器械特別審查資料申報環節合規指引(上) 為保障醫療器械臨床使用需求,進一步優化本市醫療器械審評審批程序,鼓勵以臨床價值為導向的醫療器械研發,建立更加科學、高效的醫療器械審評審批體系,在原《上海市第二類創新醫療器械特別審查程序》內容基礎上,2025年7月上海市藥品監督管理局發布《上海市第二類創新醫療器械特別審查程序》,自2025年9月1日起實施。 時間:2025-8-29 0:00:00 瀏覽量:310

-
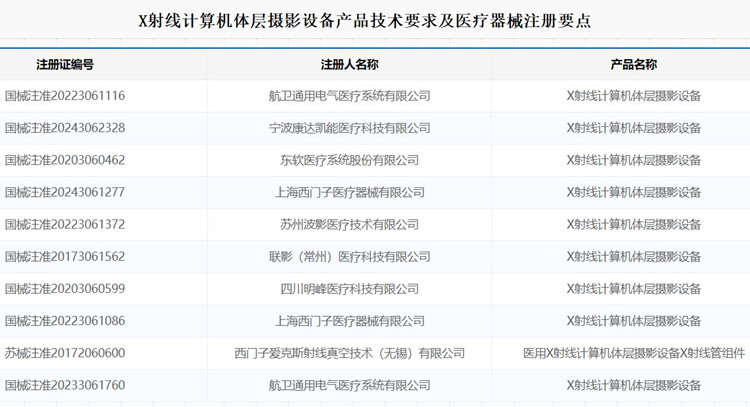
X射線計算機體層攝影設備產品技術要求及醫療器械注冊要點 用于常規 CT 檢查,支持冠狀動脈 CT 血管造影 和能譜檢查的X射線計算機體層攝影設備,在我國屬于第三類醫療器械注冊產品。該產品由掃描架、高壓發生器、X 射線管組件、光子計 數探測器、檢查床、激光定位燈、控制臺、限束器、選配 件和附件組成。一起來看X射線計算機體層攝影設備產品技術要求及醫療器械注冊要點。 時間:2025-8-28 0:00:00 瀏覽量:358
-
基孔肯雅病毒核酸檢測試劑技術審評要點(試行)(2025年第17號) 2025年8月28日,為加強醫療器械注冊申報和技術審評指導,國家藥監局器審中心組織制訂了《基孔肯雅病毒核酸檢測試劑技術審評要點(試行)》,現予發布,一起來看具體內容。 時間:2025-8-28 0:00:00 瀏覽量:381
-
遠紅外熱敷貼注冊及同品種臨床評價要點 用于緩解女性宮寒、小腹冷痛的遠紅外熱敷貼,在我國屬于第二類醫療器械注冊產品。遠紅外熱敷貼由遠紅外布、發熱袋、固定膠帶組成,發熱袋由鐵粉、活性炭、鹽、 蛭石、樹脂、水組成。該產品以非無菌狀態提供,一次性使用。本文為大家介紹 遠紅外熱敷貼注冊及同品種臨床評價要點,一起看正文。 時間:2025-8-27 0:00:00 瀏覽量:449