- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
正電子發射磁共振成像系統注冊流程和要點 參照現行《醫療器械分類目錄》,正電子發射磁共振成像系統(Imaging system of positron emission and magnetic resonance imaging,簡稱PET/MR)在我國屬于第三類醫療器械注冊產品,該類產品分類編碼為06-17-03。PET/MR根據產品結構形式不同,可分為分體式、PET插入式、完全集成式。 時間:2024/2/16 18:27:08 瀏覽量:1180

-
2024年1月國家藥監局批準醫療器械注冊產品321個 2024年國家藥監局批準醫療器械注冊產品321個,其中,境內第三類醫療器械注冊產品247個,進口第三類醫療器械注冊產品41個,進口第二類醫療器械注冊產品33個,詳見正文。 時間:2024/2/8 0:00:00 瀏覽量:1396

-
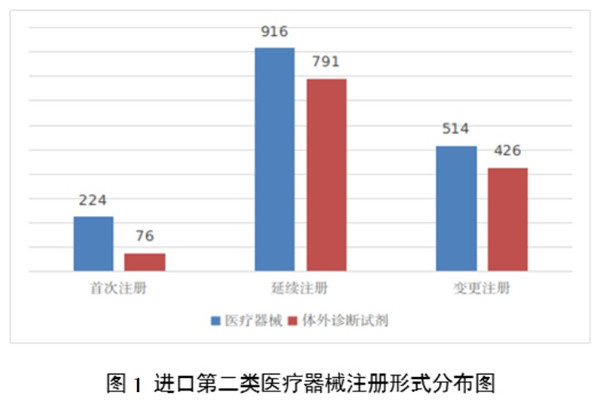
2023年進口第二類醫療器械注冊審批情況 2023年全年國家藥監局批準進口第二類醫療器械注2947項。其中,進口第二類醫療器械注冊1654項,進口第二類體外診斷試劑注冊1293項。 時間:2024/2/8 16:50:24 瀏覽量:907
-
2023年境內第二類醫療器械注冊審批情況 2023年,各省級藥品監管部門共批準境內第二類醫療器械注冊33584項,與2022年相比增加2.1%。其中,首次注冊13952項,與2022年相比增加4.6%。首次注冊項目占全部境內第二類醫療器械注冊數量的41.5%。 時間:2024/2/7 0:00:00 瀏覽量:1114

-
近視弱視用激光設備技術審評要點(2024年第6號) 2024年2月6日,為進一步規范近視弱視用激光設備的管理,國家藥監局器審中心組織制訂了《近視弱視用激光設備技術審評要點》,并于今日發布,具體內容見正文。 時間:2024/2/6 22:47:57 瀏覽量:1083

-
2023年度進口醫療器械注冊產品來源國情況 2023年度共有31個國家(地區)的進口醫療器械產品在我國獲批上市。其中,美國、德國、日本、韓國、法國醫療器械在中國醫療器械進口產品首次注冊數量位列前5位,注冊產品數量約占2023年進口產品首次注冊總數量的77%,與2022年相比略有增加。 時間:2024/2/6 0:00:00 瀏覽量:1111

-
2023年度醫療器械注冊產品品種分析 依托國家藥監局醫療器械注冊審評審批數據,帶大家一起了解2023年度醫療器械注冊產品品種,一起看看哪些品類醫療器械注冊數量靠前,哪些是熱門醫療器械注冊產品。 時間:2024/2/5 0:00:00 瀏覽量:1081

-
2023年度醫療器械注冊工作總體情況 2024年2月5日,國家藥監局發布《2023年度醫療器械注冊工作報告》,為大家介紹了2023年全年我國醫療器械注冊總體情況,一起看正文。 時間:2024/2/5 22:37:54 瀏覽量:1244

-
2024年1月浙江省醫療器械注冊審評總體情況 浙江省醫療器械注冊審評情況是醫療器械注冊人非常關心的事項,從總體情況,可以作為醫療器械注冊項目規劃的一個輸入,更加合理的預估項目風險。一起來了解2024年1月浙江省醫療器械注冊審評總體數據。 時間:2024/2/4 20:59:09 瀏覽量:960

-
樣本釋放劑產品備案時,產品應如何命名? 依據我國醫療器械分類目錄,樣本釋放劑屬于第一類醫療器械產品,應按照第一類醫療器械備案流程和要求,辦理第一類醫療器械產品備案證和第一類醫療器械生產備案憑證。但是樣本釋放劑產品有特殊性,如待測物的種類不同,備案產品應如何命名?一起看正文。 時間:2024/2/3 21:27:39 瀏覽量:1119

-
第一類醫療器械組合包類產品備案,應如何確定產品的分類編碼? 對于第一類醫療器械備案,有一類特殊的第一類醫療器械產品,即醫療器械組合包類產品,因為組合包類產品中含有多個醫療器械組分,醫療器械備案人在備案時,如何確定產品的分類編碼?一起看正文。 時間:2024/2/3 21:16:47 瀏覽量:1090

-
醫療器械臨床評價過程中單個和多個對比器械如何選擇? 對于醫療器械注冊項目來說,開展醫療器械臨床評價是基本事項之一,在醫療器械臨床評價過程中,我們如何選擇對比器械,是選擇單個醫療器械注冊產品還是多個已上市醫療器械產品?一起看本文。 時間:2024/2/2 0:00:00 瀏覽量:1016

-
國家局已批準甲型流感病毒檢測試劑注冊產品66個(截止2024年2月1日) 截至2024年2月1日,國家藥監局已批準甲型流感病毒檢測試劑共66個,其中抗原檢測產品23個、抗體檢測產品5個、核酸檢測產品38個。66個產品中,單檢產品27個,聯檢產品39個,聯檢產品多為甲流、乙流聯檢。下一步國家藥監局將持續做好甲型流感病毒檢測試劑審評審批工作,滿足當前相關傳染疫情防控需求。 時間:2024/2/2 0:00:00 瀏覽量:2246

-
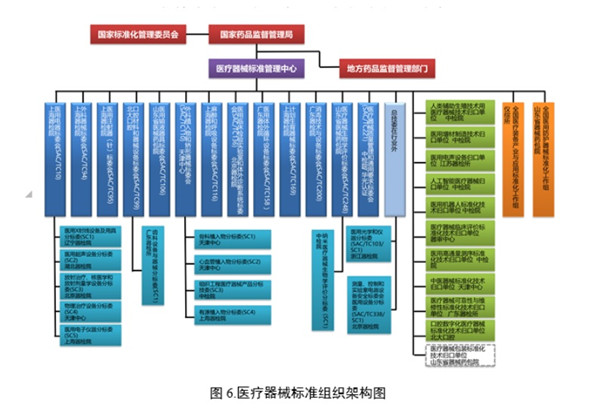
中國醫療器械標準管理年報(2023年度) 2024年2月1日,國家藥監局官網發布《中國醫療器械標準管理年報(2023年度)》,截至2023年12月31日,現行有效醫療器械標準共計1974項,其中國家標準271項,醫療器械行業標準1703項。一起來學習2023年度中國醫療器械標準情況。 時間:2024/2/1 22:03:33 瀏覽量:971
-
定制式醫療器械CE認證流程和要求 依據臨床應用的個性化需求的定制式醫療器械,如定制式隱形矯治器、定制式固定式義齒、定制式活動義齒等產品,在歐盟上市流程與常規醫療器械CE認證有較大差異,根據MDR法規,定制式醫療器械CE認證(通俗說法,不嚴謹)有特殊的流程和要求,一起看本文。 時間:2024/1/31 21:36:24 瀏覽量:1199

-
器審中心年度總結:五方面成績、五點要求 2023年1月31日,國家藥監局發布《器審中心召開2023年度總結大會暨2024年工作會議》,國家藥監局黨組成員、副局長徐景和出席會議并講話。學習國家局總結計劃會議,了解醫療器械注冊行業大勢。 時間:2024/1/31 0:00:00 瀏覽量:1208

-
無菌醫療器械注冊常見問題之滅菌工藝驗證缺陷 滅菌工藝是無菌醫療器械注冊產品質量保證的特殊工藝,直接影響產品滅菌效果。因此,滅菌工藝驗證是無菌醫療器械注冊質量管理體系核查的重點和要點,本文為大家說說滅菌工藝驗證常見問題。 時間:2024/1/30 0:00:00 瀏覽量:971

-
有源醫療器械注冊產品不同型號僅軟件功能差異,可以作為同一注冊單元嗎? 軟件的易擴展特性和數據特性,給含有軟件的有源醫療器械注冊及監管帶來挑戰。不斷的會有相關問題被醫療器械注冊人提出,藥監也不斷的在為大家答疑解惑。今天為大家說說有源醫療器械注冊產品不同型號僅軟件功能差異,是否可以作為同一注冊單元申報。 時間:2024/1/29 19:11:51 瀏覽量:1101

-
包類醫療器械注冊產品一定要有申報企業生產的組件嗎? 包類醫療器械注冊是一個特殊的注冊類別,部分包類醫療器械注冊審評技術指導原則要求包類醫療器械注冊產品中,必須至少有一種組分是企業自己生產的,但,所有包類醫療器械注冊產品都是這樣的要求嗎?其實不然。 時間:2024/1/29 18:56:21 瀏覽量:973

-
液體敷料和凝膠敷料在原材料的控制上有哪些要求? 液體敷料、凝膠敷料是今年最熱門的醫療器械注冊產品之一,在臨床和醫美領域廣泛醫用,今天我從第三方醫療器械注冊咨詢服務機構較多,給大家說說液體敷料和凝膠敷料的原材料控制要求,一起看正文。 時間:2024/1/28 17:02:01 瀏覽量:1115

