- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
電子膽道鏡注冊審評要點 電子膽道鏡在我國屬于第二類醫療器械注冊產品,產品由操作部(含吸引按鈕)、插入部(包含先端部、彎曲部和軟性部)、插頭部 和附件組成。附件包括鉗子/灌流插頭、鉗子管道開口閥。產品內置 LED 光源。與攝像系統(ETW-HD 系列或 ETF-HD 系列)配合使用,用于通過視頻監視器為胰膽系統的觀察、診斷、攝影與治療提供圖像。本文為大家介紹電子膽道鏡注冊審評要點,一起看正文。 時間:2025-6-9 20:02:03 瀏覽量:607

-
軟組織再生型疝修補補片動物試驗研究技術審評要點(征求意見稿) ?2025年6月9日,為規范技術審評要求,進一步指導注冊申請人對申報資料的準備和撰寫,國家藥監局組織制定了《軟組織再生型疝修補補片動物試驗研究技術審評要點(征求意見稿)》,并面向社會公開征求意見。 時間:2025-6-9 19:51:42 瀏覽量:526
-
流式細胞儀注冊審評要點 流式細胞儀在我國屬于第二類醫療器械注冊產品,產品基于流式細胞術原理,與配套的檢測試劑共同使用,在臨床上用于對人體血液樣本進行免疫分型。本文為大家介紹流式細胞儀注冊審評要點,一起看正文。 時間:2025-6-8 22:14:27 瀏覽量:610

-
水性聚氨酯避孕套注冊審評要點 供男性用于避孕和預防性傳播疾病的水性聚氨酯避孕套,在我國屬于第二類醫療器械注冊產品。水性聚氨酯避孕套由改性水性聚氨酯乳液制造,產品常規為薄膜套狀物,開口有卷 邊,頭部有儲精囊,套身部分為光面,顏色為無色,水性聚氨酯避孕套加二甲基硅 油作為潤滑劑。該產品以非無菌狀態提供。本文為大家介紹水性聚氨酯避孕套注冊審評要點,一起看正文。 時間:2025-6-8 22:05:38 瀏覽量:745

-
醫療器械注冊資料之“申報產品適用標準情況”應包括哪些內容? ?醫療器械注冊產品在首次注冊申報時,在產品技術要求及檢驗報告項目下,需要提交“申報產品適用標準情況”,具體應包括哪些內容?一起看正文。 時間:2025-6-7 17:37:05 瀏覽量:612

-
適用YY 0648的臨床檢驗器械是否需要適用GB/T 42125.14-2023? 臨床檢驗器械注冊產品是醫療器械大家族中的重要類別,與體外診斷試劑一起構成了醫療器械的半壁江山。本文為大家說說臨床檢驗器械注冊檢驗時,適用YY 0648的臨床檢驗器械是否需要適用GB/T 42125.14-2023?一起看正文。 時間:2025-6-7 17:28:29 瀏覽量:646

-
第二類醫療器械(腦電圖機)注冊審評要點 供人體腦電生理信號檢測、處理、顯示和儲存使用的腦電圖機,在我國屬于第二類醫療器械注冊產品。腦電圖機由腦電放大器、電源適配器、USB 數據線、電腦端軟件、硬件加密鎖組成。本文為大家介紹腦電圖機注冊審評要點,一起看正文。 時間:2025-6-5 22:42:59 瀏覽量:662

-
關于對藥品醫療器械質量安全內部舉報人舉報實施獎勵的公告(2025年第41號) 2025年6月5日,國家藥監局、財政部、市場監管總局聯合發布《關于對藥品醫療器械質量安全內部舉報人舉報實施獎勵的公告(2025年第41號)》,公告的發布,更是提醒藥品企業、醫療器械注冊人、醫療器械生產企業建立合規、透明醫療器械質量管理體系的必要性,及醫療器械產品形式合規、實際合規的重要性,一起來看具體內容。 時間:2025-6-5 22:32:45 瀏覽量:512

-
醫用透明質酸鈉液體敷料注冊審評要點 醫用透明質酸鈉液體敷料是最熱門、最廣為人知的醫美類醫療器械注冊產品之一,醫用透明質酸鈉液體敷料通過在創面表面形成保護層,起物理屏障作用,用于非慢性創面及其周圍皮膚的護理。本文為大家介紹醫用透明質酸鈉液體敷料注冊審評要點,一起看正文。 時間:2025-6-4 22:38:17 瀏覽量:997

-
山東省第二類醫療器械注冊審批等5個事項6月起實行電子證照 實行電子證照是國內及各地藥監近年改革事項之一,來自山東省藥品監督管理局披露的消息,自2025年6月1日起,山東省藥監局受理的國產第二類醫療器械注冊審批等5個事項實行電子證照。這標志著山東省藥監局電子證照實施工作圓滿收官,實現了全部23大類注冊許可事項電子證照“全覆蓋”。 時間:2025-6-3 18:15:08 瀏覽量:823

-
醫用重組膠原蛋白液體敷料注冊審評要點 ?適用于淺表性創面及周圍皮膚的護理的醫用重組膠原蛋白液體敷料,在我國屬于第二類醫療器械注冊產品。醫用重組膠原蛋白液體敷料由重組膠原蛋白、甘油、1,3-丁二醇、卡波姆 940、三乙 醇胺、對羥基苯乙酮和注射用水組成,以西林瓶封裝。該產品以無菌狀態提供,經 輻照滅菌,一次性使用。本文為大家介紹醫用重組膠原蛋白液體敷料注冊審評要點。 時間:2025-6-2 20:10:02 瀏覽量:819

-
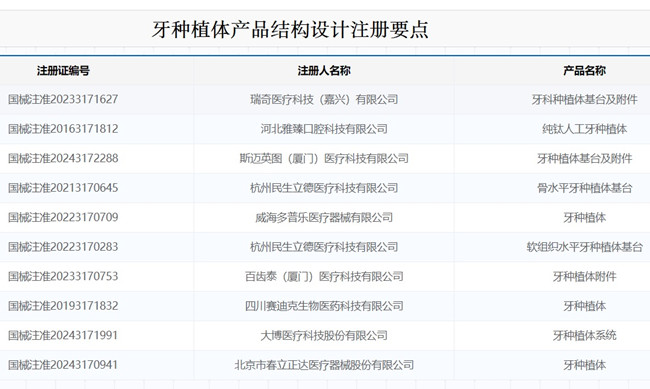
牙種植體產品結構設計注冊要點 牙種植體在我國屬于第三類醫療器械注冊產品,適用于牙缺失患者的種植修復,是用外科方法將種植體植入到牙槽骨內,用于為義齒等修復體提供固定或支撐,以恢復患者的咀嚼功能。本文為大家介紹牙種植體產品結構設計注冊要點,一起看正文。 時間:2025-6-2 19:58:05 瀏覽量:700
-
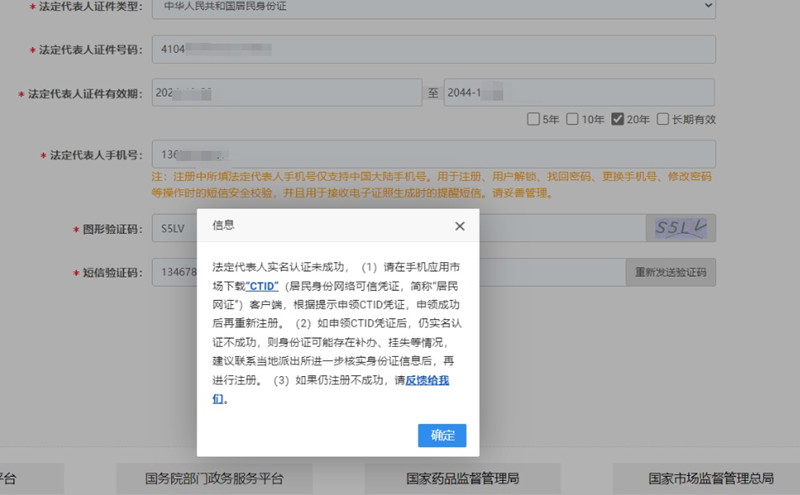
第一類醫療器械產品備案系統注冊時,法定代表人實名認證未成功怎么辦? 這兩天正好有遇到客戶在申請第一類醫療器械產品備案,在注冊系統賬號時,法定代表人實名認證不通過,提示“法定代表人實名認證未成功”,遇到這種情況怎么處理,我來說說我的經歷和處理過程。 時間:2025-5-30 14:56:04 瀏覽量:703
-
在使用醫療器械前,為什么要仔細閱讀說明書? ?對于醫療器械注冊產品來說,醫療器械說明書是非常重要的文件之一,醫療器械說明書不僅僅是使用的說明,更是安全用械必讀文件。本文為大家說說為什么要仔細閱讀說明書,一起看正文。 時間:2025-5-28 22:23:54 瀏覽量:974

-
2025年4月廣西藥監局批準61個第二類醫療器械注冊產品 來自廣西壯族自治區藥品監督管理局近日披露的數據,2025年4月共計批準61個第二類醫療器械注冊產品,其中,第二類醫療器械變更注冊18項,第二類醫療器械延續注冊9項,第二類醫療器械新注冊33項,一起來看具體哪些產品獲批。 時間:2025-5-27 22:40:01 瀏覽量:917

-
如何判斷“導管鞘”產品的管理類別? ?判斷擬注冊器械的管理屬性和管理類別,是醫療器械注冊項目策劃階段的關鍵工作之一。特別是對“導管鞘”這樣管理類別相對復雜的產品,今天寫個文章說說這個事。 時間:2025-5-26 21:05:42 瀏覽量:635

-
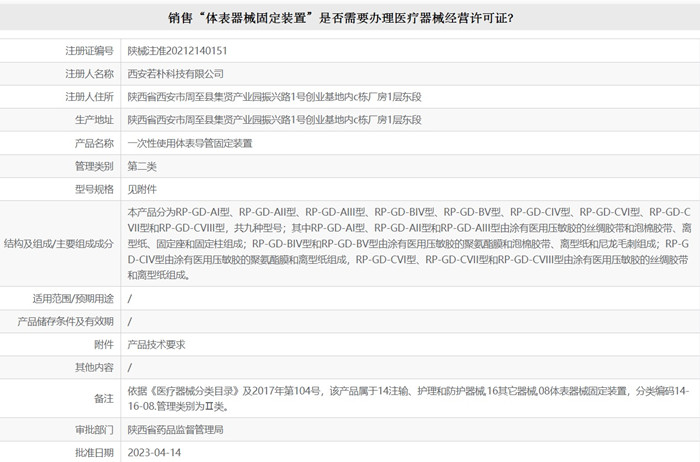
銷售“體表器械固定裝置”是否需要辦理醫療器械經營許可證? ?體表固定裝置通常是能專門為某一種或某一類器械的使用提供固定的裝置,用于固定使用過程中的醫療器械。今天正好有客戶打電話問到我,銷售“體表器械固定裝置”是否需要辦理醫療器械經營許可證?考慮到“體表器械固定裝置”是否屬于醫療器械需要視情況判定,因此,寫個文章給大家說說這個事。 時間:2025-5-26 20:57:56 瀏覽量:512
-
醫療器械包裝標簽上“失效日期”的格式和要求 ?對于醫療器械注冊人或是醫療器械生產企業來說,醫療器械說明書和標簽違規是最頻繁發生的違規類型之一,本文為大家說說醫療器械包裝標簽上“失效日期”的格式和要求,一起看正文。 時間:2025-5-25 23:09:59 瀏覽量:1371

-
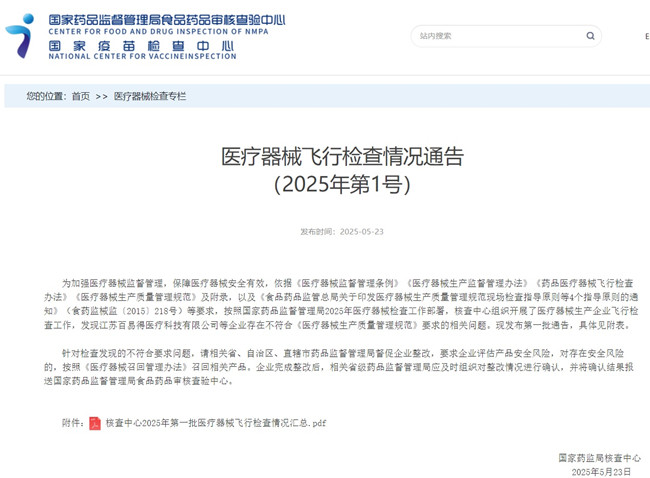
國家藥監局醫療器械飛行檢查發現18家醫療器械企業體系不符合要求 2025年5月23日,國家藥監局發布《醫療器械飛行檢查情況通告(2025年第1號)》,按照國家藥品監督管理局2025年醫療器械檢查工作部署,核查中心組織開展了醫療器械生產企業飛行檢查工作,發現江蘇百易得醫療科技有限公司等企業存在不符合《醫療器械生產質量管理規范》要求的相關問題。 時間:2025-5-24 0:00:00 瀏覽量:838
-
上海市醫療器械生產許可證申請時,生產地址是否要包含研發區域、辦公區域? 對于上海市醫療器械生產許可證申請時,企業要提供生產地址、生產場地布局和場地面積等相關資料和信息。今天有上海市醫療器械注冊人問到,生產地址是否要包含研發區域、辦公區域?寫個文章,說說這個事。 時間:2025-5-23 18:54:44 瀏覽量:698

