- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
以醫療器械作用為主的藥械組合產品中藥物定性定量及體外釋放研究注冊審查指導原則 以醫療器械作用為主的藥械組合產品中藥物定性、定量及體外釋放研究注冊審查指導原則 時間:2022-1-19 0:00:00 瀏覽量:2143

-
人工晶狀體注冊審查指導原則(2022年第4號) 2022年1月17日,藥監總局發布《人工晶狀體注冊審查指導原則(2022年第4號)》,原則的發布,將為有志于愿意中長期投資、深耕醫療行業的企業家們提供指引,增加確信。 時間:2022-1-18 19:24:04 瀏覽量:2281
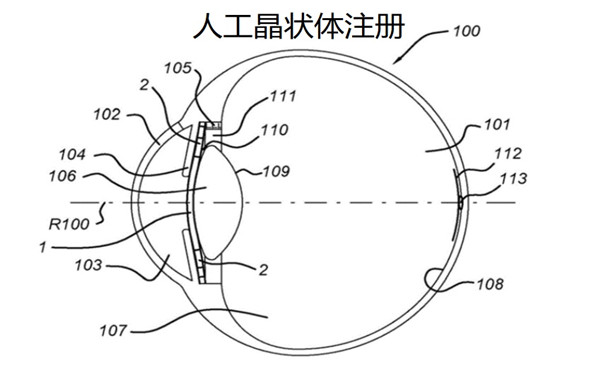
-
一次性使用內窺鏡注射針注冊審查指導原則(2022年第4號) 2022年1月17日,藥監總局發布《一次性使用內窺鏡注射針注冊審查指導原則(2022年第4號)》,一次性使用內窺鏡注冊產品,避免了臨床重復應用過程的消毒,其便捷性有可能讓其成為臨床應用趨勢。 時間:2022-1-18 19:16:13 瀏覽量:3016

-
可降解鎂金屬骨科植入物注冊審查指導原則(2022年第4號) 2022年1月17日,藥監總局發布《可降解鎂金屬骨科植入物注冊審查指導原則(2022年第4號)》,詳見正文。 時間:2022-1-18 0:00:00 瀏覽量:2379

-
肺結節CT影像輔助檢測軟件注冊審查指導原則(征求意見稿) 肺結節CT影像輔助檢測軟件注冊審查指導原則(征求意見稿) 時間:2022-1-16 12:39:07 瀏覽量:2593

-
體外診斷試劑注冊發補共性問題分析 以上海市體外診斷試劑注冊發補共性問題為例,為大家分享常見發補事項,及如何規避出現此類問題,為體外診斷試劑成功注冊提供保證。 時間:2022-1-16 12:06:47 瀏覽量:2351

-
上海醫療器械注冊立卷審查常見問題分析 2021年8月20日,上海市器審中心啟動了對第二類醫療器械首次注冊立卷審查試行工作,截至11月30日共對92件首次醫療器械注冊?申請資料開展了立卷審查。其中一次通過立卷審查受理49件(占比53.2%),立卷審查發補39件(占比42.4%,其中有源21件、無源15件、IVD3件),企業提出撤審3件(占比3.3%),不予受理1件(占比1.1%)。本文對常見問題進行歸納匯總,供相關企業注冊人員參考。 時間:2022-1-16 11:57:26 瀏覽量:2334

-
臨平區支持產業高質量發展政策的實施意見,共99條 朋友問到這個,然后去了解到,臨平有這么多實打實的、看得見、夠得著的惠企政策。不說多,直接附上政策文件;一句話:歡迎來到臨平。 時間:2022-1-14 16:43:15 瀏覽量:3692

-
保健食品人群試食試驗倫理審查工作指導原則(2022年版) 為規范保健食品人群試食試驗倫理審查工作,根據《中華人民共和國食品安全法》及其實施條例、《保健食品注冊與備案管理辦法》及其配套文件以及《涉及人的生物醫學研究倫理審查辦法》等相關規定,制定本指導原則。 時間:2022-1-14 11:55:01 瀏覽量:2569

-
關于發布允許保健食品聲稱的保健功能目錄非營養素補充劑(2022年版)及配套文件的公告(征求意見稿) 為進一步推進保健食品注冊工作,根據《中華人民共和國食品安全法》《保健食品注冊與備案管理辦法》《保健食品原料目錄和功能目錄管理辦法》,市場監管總局組織制定了《關于發布〈允許保健食品聲稱的保健功能目錄 非營養素補充劑(2022年版)〉及配套文件的公告(征求意見稿)》,現面向社會公開征求意見,意見建議反饋截止時間為2022年2月12日。 時間:2022-1-14 11:49:05 瀏覽量:2550
-
2021年12月進口第一類醫療器械產品備案信息 2022年1月11日,藥監總局發布《2021年12月進口第一類醫療器械產品備案信息》公告,2021年最后一個月藥監總局完成醫用絲綢膠帶、醫用檢查手套等156個盡快醫療器械產品備案項目審批。 時間:2022-1-13 0:00:00 瀏覽量:4688

-
各省醫療器械許可備案相關信息(截至2021年12月31日) 近日,藥監總局公布各省醫療器械許可備案相關信息,江蘇、廣東、北京、浙江、上海醫療器械注冊證數量分列前五位。 時間:2022-1-13 17:24:36 瀏覽量:2099
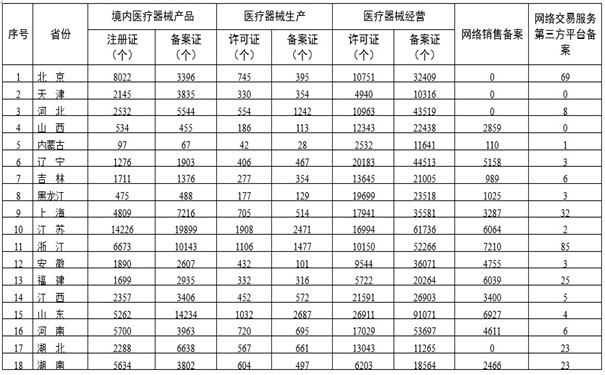
-
2021年11月上海市第二類醫療器械注冊技術審評用時情況 2021年11月上海市第二類醫療器械注冊?技術審評用時情況 時間:2022-1-13 17:17:04 瀏覽量:2059
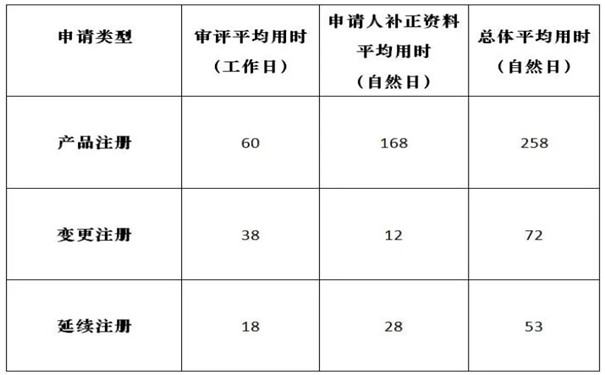
-
醫療器械產品不同批次研究資料等共性問題解答 醫療器械產品不同批次研究資料等共性問題是近期高頻醫療器械注冊咨詢?事項,官方解答正文所示。 時間:2022-1-12 15:46:28 瀏覽量:2272

-
藥監總局醫療器械注冊審評長三角分中心老師聯系電話 藥監總局醫療器械注冊?審評長三角分中心老師聯系電話 時間:2022-1-12 15:40:20 瀏覽量:3794

-
大灣區醫療器械注冊審評老師聯系電話 大灣區醫療器械注冊審評老師聯系電話 時間:2022-1-12 15:35:30 瀏覽量:4322

-
醫療器械說明書更改告知審查申請等共性問題解答 醫療器械說明書更改告知審查申請等共性問題解答 時間:2022-1-10 15:47:01 瀏覽量:2331

-
江蘇二類醫療器械注冊符合條件可當日拿證 2022年1月8日,江蘇省人民政府辦公廳印發《關于優化審評審批服務推動創新藥械使用促進醫藥產業高質量發展的行動方案(2022-2024年)》,對醫療器械注冊審批時限優化,審評審批服務體系提升等提出具體行動目標和多項有力措施。其中,2022年6月底前,同一集團企業在境內已注冊的第二類醫療器械來蘇申報的,5個工作日完成技術審評,符合要求的當日發放注冊證。 時間:2022-1-10 15:17:15 瀏覽量:2686

-
液體膏狀敷料將不能按照一類醫療器械備案申報 2021年12月31日消息,NMPA對外發布《第一類醫療器械產品目錄》。據悉,《第一類醫療器械產品目錄》自2022年1月1日起正式施行。液體膏狀敷料將不能按照一類醫療器械備案申報。 時間:2022-1-7 9:47:16 瀏覽量:3603

-
浙江發布實施醫療器械唯一標識工作推進方案 ?為貫徹落實國家藥監局于2021年9月印發的《關于做好第二批實施醫療器械唯一標識工作的公告》,浙江省藥品監督管理局、浙江省衛生健康委員會、浙江省醫療保障局三部門聯合印發《浙江省推進實施醫療器械唯一標識 (UDI)工作方案》。 時間:2022-1-7 9:37:36 瀏覽量:3152

