- 關(guān)于我們
- 公司簡(jiǎn)介
- 聯(lián)系我們
- 聯(lián)系我們

聯(lián)系電話:0571-86198618手機(jī): 18058734169 (微信同)手機(jī):18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
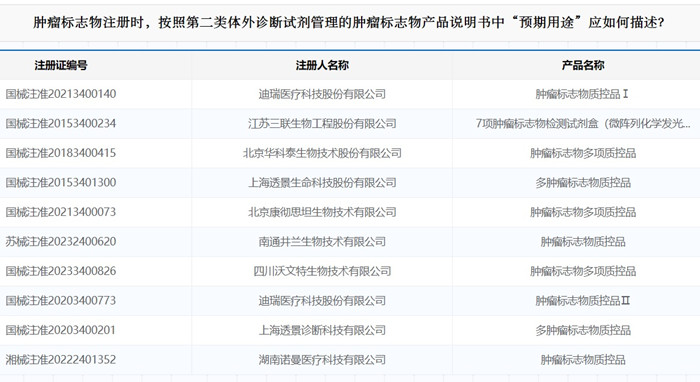
腫瘤標(biāo)志物注冊(cè)時(shí),按照第二類體外診斷試劑管理的腫瘤標(biāo)志物產(chǎn)品說(shuō)明書中“預(yù)期用途”應(yīng)如何描述?
首先應(yīng)符合《體外診斷試劑說(shuō)明書編寫指導(dǎo)原則(2023年修訂版)》的要求,預(yù)期用途分為三段內(nèi)容,首段內(nèi)容詳細(xì)說(shuō)明檢測(cè)的分析物、檢測(cè)類型、樣本類型;第二段應(yīng)詳細(xì)說(shuō)明預(yù)期用途。包括適用人群,相關(guān)的臨床適應(yīng)證和檢測(cè)目的等;其余段落對(duì)被測(cè)分析物進(jìn)行背景介紹、說(shuō)明相關(guān)的臨床或?qū)嶒?yàn)室診斷方法說(shuō)明與預(yù)期用途相關(guān)的臨床背景情況;說(shuō)明被測(cè)分析物與臨床適應(yīng)證的關(guān)系。此外,還應(yīng)符合《腫瘤標(biāo)志物類定量檢測(cè)試劑注冊(cè)審查指導(dǎo)原則(2023年修訂版)》的要求,首段內(nèi)容還應(yīng)增加“主要用于對(duì)惡性腫瘤患者進(jìn)行動(dòng)態(tài)監(jiān)測(cè)以輔助判斷疾病進(jìn)程或治療效果,不能作為惡性腫瘤早期診斷或確診的依據(jù),不用于普通人群的腫瘤篩查”。
